Кузнецов A. E. Научные основы экобиотехнологии . Раздел 1
Кузнецов A. E. Научные основы экобиотехнологии . Страница 87
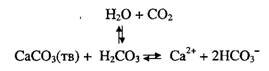
При снижении содержания CO2 снижается и содержание H2CO3, осаждается карбонат кальция. В нейтральных и слабощелочных водах, где карбонатная система служит рН-задающей, рН меняется в интервале 6,0-8,5.
На изменение рН могут влиять минеральные породы, с которыми соприкасается вода. В различных частях водной экосистемы может возникать кислотно-щелочная зональность.
рН (>8,5) сильнощелочных вод обусловлен присутствием соды (NaHCO3, реже Na2CO3). Такие воды характерны для лесостепной зоны и саванны.
В формировании рН среды может участвовать не только карбонатная система, но и другие кислоты и основания: CH3COOH, NH/ - NH3,
Si(OH)4 - SiO(OH)3", H2PO4" - HPO42', H2S - HS", органические соединения с кислотными и основными группами, такие как аминокислоты и другие азотсодержащие соединения, карбоновые кислоты, серусодержащие соединения. Типичные концентрации низкомолекулярных лигандов в природных водах следующие: HCO3" (CO32") - 3. IO"3 М, CH3COOH - IO"4 М, NH/ (NH3) - IO"5 М, Si(OH)4 (SiO(OH)3") -5-10"4 М, H2PO4" (HPO42") - IO"5 М, H2S (SbT) - IO"5 М.
В регулировании рН участвуют также фотосинтез и дыхание. Поглощение CO2 в процессе фотосинтеза приводит к уменьшению количества H2CO3 и H+, т.е. к повышению рН. При дыхании, наоборот, увеличивается содержание CO2 и снижается рН. Поэтому рН воды в водоемах колеблется в течение суток: ночью рН понижается, днем повышается. Амплитуда колебаний рН может составить две единицы и более.
Окислительно-восстановительный потенциал Eh (редокс потенциал) характеризуется концентрацией окислителя в среде: чем выше его концентрация, тем выше потенциал.
Существуют верхнее и нижнее теоретические значения Eh, за пределами которых вода как химическое соединение становится термодинамически неустойчивой, т.е. окисляется с выделением кислорода либо восстанавливается с выделением водорода.
